

La estabilidad de los medicamentos es uno de los desafíos más críticos en la industria farmacéutica. Los productos farmacéuticos van desde fármacos de moléculas pequeñas sintetizados químicamente hasta biológicos complejos derivados de organismos vivos o procesos biotecnológicos. Debido a sus diferentes características físicas y químicas, estos fármacos responden de manera muy diferente a las variaciones de temperatura.

En las pruebas y el almacenamiento farmacéuticos, la temperatura no es una condición de fondo, es un factor de estabilidad clave que afecta directamente la seguridad, la eficacia y la vida útil de los medicamentos.
Los medicamentos biológicos son particularmente sensibles a la temperatura debido a sus estructuras basadas en proteínas:
Los aumentos leves de la temperatura pueden causar desnaturalización de las proteínas
La deformación estructural puede resultar en la pérdida de actividad farmacológica
Una vez desnaturalizada, la actividad biológica es a menudo irreversible
Incluso pequeñas desviaciones de temperatura durante las pruebas o el almacenamiento pueden comprometer la eficacia del producto.
Para ciertas preparaciones líquidas, las temperaturas excesivamente bajas también pueden presentar riesgos:
Los solutos pueden cristalizar bajo condiciones de baja temperatura
Las relaciones de concentración pueden cambiar, afectando la precisión de la dosis
La cristalización puede bloquear las agujas de inyección y aumentar el riesgo del paciente
Estos problemas destacan la necesidad de entornos de temperatura controlados y repetibles durante la evaluación de estabilidad.
Los medicamentos diseñados para el almacenamiento a largo plazo están expuestos continuamente a cambios de temperatura ambiental durante el almacenamiento, el transporte y el manejo diario. Con el tiempo, incluso los ciclos de temperatura pequeños y repetidos pueden actuar como un factor de degradación acumulativa, lo que lleva a:
Degradación química
Aumento de los niveles de impureza
Eficacia terapéutica reducida
Esto hace que el control de temperatura sea un protector de calidad a largo plazo, no solo un requisito de prueba a corto plazo.
Durante el desarrollo temprano de fármacos, la incertidumbre es inevitable.Cámaras de temperaturaSon herramientas esenciales para el cribado de la formulación y la comparación de la estabilidad en esta etapa.

Las aplicaciones típicas en I + D incluyen:
Evaluación del comportamiento de la formulación bajo estrés a altas y bajas temperaturas
Simulando ciclos de temperatura diarios o estacionales
Comparación de la estabilidad estructural en múltiples candidatos compuestos
Al observar los cambios físicos y químicos en condiciones de temperatura controlada, los investigadores pueden identificar formulaciones con estructuras estables y un rendimiento confiable, proporcionando una base sólida para un mayor desarrollo.
Cámara de prueba de alta temperatura bajaSiguen siendo indispensables en todos los procesos de fabricación farmacéutica y garantía de calidad.
Las materias primas entrantes se evalúan rutinariamente en condiciones de temperatura controlada. Por ejemplo, la calidad de la gelatina de la cápsula puede variar debido a las diferencias de temperatura durante el procesamiento aguas arriba. Las cámaras de temperatura ayudan a verificar si la gelatina mantiene un rendimiento gelificante constante en condiciones de temperatura estándar y extremas antes de ser aprobada para uso en producción.
En la producción de antibióticos, la temperatura de fermentación influye directamente en la consistencia del ingrediente activo. Incluso pequeñas desviaciones de temperatura pueden conducir a la variabilidad del lote. Al simular diferentes escenarios de temperatura de fermentación en unCámara de temperatura constante, Los fabricantes pueden:
Analizar el impacto de la temperatura en el rendimiento del ingrediente activo
Optimizar los parámetros del proceso
Garantizar la coherencia entre lotes
La validación de este proceso es esencial para mantener una calidad estable del fármaco a escala.
Las cámaras de temperatura continúan desempeñando un papel vital después de que las drogas ingresan al mercado. De acuerdo con los requisitos reglamentarios, las empresas farmacéuticas realizan habitualmente estudios de estabilidad posteriores a la comercialización utilizando muestras de mercado.
Estos estudios suelen involucrar:
Exposición a largo plazo bajo condiciones de almacenamiento controladas
Pruebas periódicas para el crecimiento de impurezas y la pérdida de potencia
Recopilación de datos para inspección regulatoria y auditoría
Si se detectan anomalías, los fabricantes pueden ajustar rápidamente las recomendaciones de almacenamiento o iniciar acciones correctivas, minimizando los riesgos para la seguridad del paciente.
La Evaluación de la estabilidad farmacéutica se basa principalmente en dos enfoques de prueba complementarios.
Las pruebas de estabilidad aceleradas simulan el envejecimiento prolongado del fármaco en un período de tiempo más corto mediante la aplicación de condiciones de temperatura elevada y humedad controlada.
Los objetivos típicos incluyen:
Predecir las posibles vías de degradación
Estimación de la vida útil durante el desarrollo temprano
Apoyar las decisiones de selección de fórmulas
Este método mejora significativamente la eficiencia de I + D al tiempo que proporciona datos predictivos valiosos.
Las pruebas de estabilidad a largo plazo registran cambios en tiempo real en condiciones cercanas a los entornos de almacenamiento reales. Estos datos son esenciales para:
Determinación de fechas de vencimiento precisas
Optimización de las condiciones de almacenamiento y transporte
Apoyo a las presentaciones y aprobaciones regulatorias
Los estudios de estabilidad farmacéutica se llevan a cabo dentro de marcos regulatorios bien establecidos para garantizar la confiabilidad de los datos y la aceptación global. Las pautas comúnmente referenciadas incluyen:
ICH Q1A(R2)-Pruebas de estabilidad de nuevas sustancias y productos farmacológicos
ICH Q1B-Pruebas de fotoestabilidad de nuevos productos y sustancias farmacéuticas
GMPRequisitos para el control ambiental y la trazabilidad de los datos
Las cámaras de temperatura utilizadas en las pruebas farmacéuticas deben respaldar condiciones estables, repetibilidad y registros de datos completos para cumplir con estas expectativas regulatorias.
Para las pruebas de estabilidad farmacéutica, las cámaras de temperatura generalmente proporcionan las siguientes características de rendimiento:
Rango de temperatura:-20 °C a 60 °C(Personalizable)
Fluctuación de la temperatura:± 0,5 °C
Uniformidad de la temperatura:± 2 °C
Modos de prueba: estabilidad acelerada y estabilidad a largo plazo
Registro de datos: registro continuo para Auditoría y Cumplimiento
Estos parámetros garantizan condiciones de exposición consistentes y resultados de pruebas fiables.
Las cámaras de temperatura de la industria LIB ofrecen entornos de temperatura estables y repetibles para pruebas de estabilidad farmacéutica.
Fluctuación de temperatura: ± 0,5 °C
Uniformidad de temperatura: ± 2 °C
Apoya: estudios de estabilidad acelerados y a largo plazo
Registro de datos: registros continuos de temperatura y humedad
Modelo | T-100 | T-225 | T-500 | T-1000 |
Volumen interior | 100L | 225L | 500L | 1000L |
Carga de calor | 1000W | |||
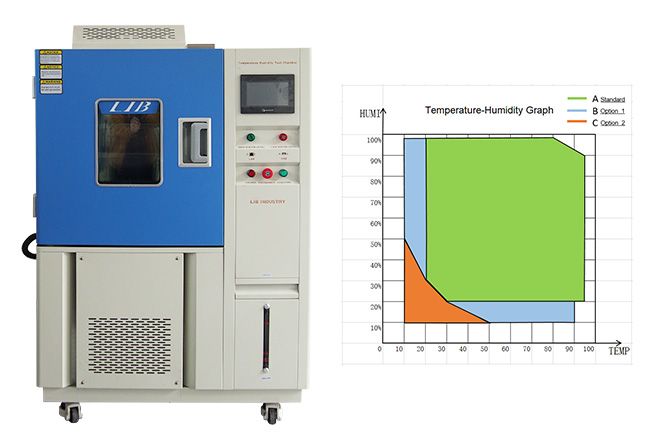
Rango de temperatura | A : -20 °C ~ 150 °C B : -40 °C ~ 150 °C C: -70 °C ~ 150 °C | |||
Fluctuación de la temperatura | ± 0,5 ℃ | |||
Desviación de la temperatura | ± 2,0 ℃ | |||
Tasa de enfriamiento | 1 ℃ / min | |||
Tasa de calefacción | 3 ℃ / min | |||
Sistema de enfriamiento | Refrigerante respetuoso con el medio ambiente, compresor francés TECUMSEH, que cumple con los requisitos de los estándares GWP | |||
Controlador | Controlador de pantalla táctil LCD a color programable, conexión Ethernet | |||
 | ||||
Estas capacidades ayudan a los fabricantes farmacéuticos a generar datos de estabilidad confiables, reducir la desviación de las pruebas y cumplir con los requisitos de inspección regulatoria con confianza.
Las cámaras de temperatura de la industria LIB admiten programas de estabilidad de I + D, fabricación y poscomercialización de productos farmacéuticos al combinar un control preciso de la temperatura, un diseño orientado al cumplimiento, y registros de datos rastreables, lo que ayuda a los fabricantes a proteger la calidad del producto y la seguridad del paciente durante todo el ciclo de vida del producto.
Póngase en contacto con la industria LIBInquiry@libtestchamber.comPara obtener una conformidadCámara de temperaturaSolución dentro de 1 ~ 3 horas para pruebas de estabilidad farmacéutica en I + D, producción y programas de estabilidad.
 English
English русский
русский français
français العربية
العربية Deutsch
Deutsch Español
Español 한국어
한국어 italiano
italiano tiếng việt
tiếng việt ไทย
ไทย Indonesia
Indonesia

.webp)
